Instrucciones
Usted tiene las siguientes opciones en este simulador para moléculas pequeñas tanto inorgánicas como orgánicas.
- En la parte superior, aparecen los botones 2D y 3D para que pueda observar el modelo en dos o tres dimensiones.
- A continuación se presenta el modelo en dos o tres dimensiones.
- "Search" puede ser utilizado para buscar alguna molécula, escribiendo el nombre en inglés, por ejemplo al escribir, sulphuric acid (ácido sulfúrico).
- Color de fondo, sirve seleccionar el color del fondo del modelo en tres dimensiones.
- Girar X, Y, Z, para girar el modelo en tres dimensiones en los ejes x, y, z.
- Alambres, varillas y pelotas y varillas, para cambiar el modelo en tres dimensiones en esas representaciones.
- Energía, aparce en la parte superior la energía de la molécula en kJ/mol o kcal/mol.
- Minmizar por MMFF94, normalmente las estructuras iniciales que se crean en los simuladores poseen energías mucho mayores a las que tendría un objeto real, por esta razón, se utilizan algoritmos para calcular las posiciones y fuerzas originales, con el objetivo de minimizarlas y que sean más realistas.
- Arrastrar Minimizar, usted puede arrastrar un átomo, soltarlo y entonces el sistema hace un cálculo de minimización de energía.
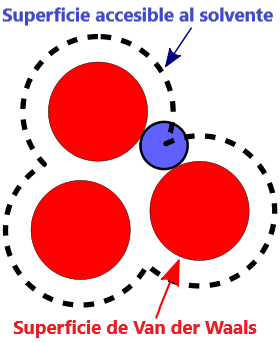
- Superficie VDW, La superficie de van der Waals de una molécula es una representación abstracta o modelo de esa molécula, que ilustra dónde, en términos muy generales, podría haber una superficie para la molécula en función de los cortes duros de los radios de van der Waals para átomos individuales, y representa una superficie a través de la cual la molécula podría concebirse interactuando con otras moléculas.
- PEM es el mapa de potencial electrostático.
- Cargas parciales, para ver el valor de la carga relativa positiva o negativa de cada átomo.
- Tetraedros, para el caso que exista alguna átomo tetraédrico.
- Dipolos enlaces, para ver el los dipolos de todos los enlaces.
- Dipolo molecular, para ver el momento dipolar resultante de toda la molécula.
- Botón 2D, cuando escoge el botón 2D, la aplicación tiene su propio menú y quedan inhabilitados todos los botones 3D.
Laboratorio de IA: Tu Copiloto de Estudio
Aprende a usar la Inteligencia Artificial
La IA (como ChatGPT, Gemini o Copilot) no sirve solo para darte respuestas. Úsala para entender mejor. Aquí tienes 3 "Prompts" (instrucciones) maestros para probar ahora mismo:
1. El "Traductor" de Conceptos
Úsalo cuando la teoría sea confusa.
2. El Generador de Retos
Para practicar antes del examen.
3. El Tutor Socrático
Cuando te trabes en un ejercicio.
Soluciones

Podcast: Entendiendo la Molalidad
Escucha la explicación conceptual sobre por qué usamos Kg de solvente.
Video Explicativo
Presentación Resumida
Para mejor experiencia en celular, abre la guía directamente:
Abrir Guía PDFVisualiza las diapositivas clave del tema.
Infografía Resumen

Guía visual rápida sobre conceptos clave.
Antes de empezar...
Para dominar este tema, asegúrate de tener claros estos conceptos:
- Solvente (kg) vs Solución (L): La diferencia #1. Aquí pesamos el solvente, no medimos el volumen total.
- Masa Molar: Seguiremos usándola (g/mol) para convertir gramos a moles.
- Temperatura: Recuerda que el volumen cambia si hace calor o frío; la masa NO cambia.
Futuros Médicos
¿Qué es la Osmolalidad? Es la medida de la concentración total de partículas disueltas en 1 kg de agua (mOsm/kg). A diferencia de la molalidad simple, aquí importa el número de partículas osmoactivas: por ejemplo, 1 mol de NaCl genera 2 Osmoles (Na+ y Cl-).
¿Por qué es el estándar médico? Porque usamos masa (kg) en lugar de volumen. Un paciente con fiebre (40°C) dilata el volumen de su sangre, falsificando la Molaridad. La Osmolalidad es inmune a la temperatura, garantizando datos críticos reales.
Ejemplo Real: El agua se expande aprox. 0.5% al pasar de 20°C (lab) a 37°C (cuerpo). Esto haría que una medición de Sodio de 140 mM varíe casi 1 mM solo por temperatura. ¡En casos críticos, esa precisión es vital!
Físicos e Ingenieros
El reto térmico: ¿Cómo diseñar un anticongelante para un motor que va de -20°C a 100°C?
Si usaras Molaridad (mol/L), tu "concentración" cambiaría simplemente porque el líquido se expande con el calor. Necesitas una unidad a prueba de temperatura: la Molalidad.
El Problema: La Lupa de la Temperatura
Imagina que preparas una solución 1.0 Molar exacta a las 7:00 AM (fío). A medio día (calor), el líquido se dilata (ocupa más espacio).
Resulta que tienes los mismos moles, pero en más litros. ¡Tu Molaridad bajó sin que tocaras el matraz!
Para experimentos de alta precisión, y propiedades coligativas (como el punto de congelación), esto es inaceptable. Por eso usamos Molalidad (m): moles por kilogramo de solvente. La masa no cambia con el clima.
Molalidad (m)
La concentración molal o molalidad, se abrevia como m y se define como el número de moles de soluto por kilogramo de solvente.
| n (moles de soluto) |
| kg (masa de solvente) |
Ejemplo N° 1 (Paso a Paso)
Calcular la concentración molal de una solución que contiene 18.0 g de NaOH en 100
mL
de
agua.
Datos: Masa Molar NaOH = 40.0 g/mol; Densidad del agua = 1.00 g/mL (aprox).
Procedimiento (Método del Factor Unitario en 1 Paso):
Opción Fórmula: m = n / kg (directa
pero propensa a errores).
Opción Recomendada: Línea de
Razonamiento (análisis dimensional seguro).
Razonamiento: Partimos de la relación que tenemos (gramos/volumen) y transformamos ambas unidades simultáneamente usando factores de conversión:
- El numerador: Gramos NaOH → Moles NaOH (usando la Masa Molar).
- El denominador: mL Agua → Gramos Agua (densidad) → Kilogramos Agua.
| 18.0 g NaOH | x | 1 mol NaOH | x | 1 mL Agua | x | 1000 g Agua | = 4.50 m |
| 100 mL Agua | 40.0 g NaOH | 1.00 g Agua | 1 kg Agua |
Nota: Cancelamos (g NaOH), (mL Agua) y (g Agua), quedando mol/kg.
Ejemplo N° 2 (Soluto Sólido, Solvente en Masa)
Se disuelven 10.0 g de Glucosa (C6H12O6) en 200. g
de Agua. Calcular la molalidad.
Datos: Masa Molar Glucosa = 180. g/mol.
Procedimiento:
Opción Fórmula: m = n / kg
Opción Recomendada: Línea de
Razonamiento (factor unitario).
Razonamiento: Convertimos numerador (g → moles) y denominador (g → kg) en un solo paso.
| 10.0 g Glucosa | x | 1 mol Glucosa | x | 1000 g Agua | = 0.278 m |
| 200. g Agua | 180. g Glucosa | 1 kg Agua |
Ejemplo N° 3 (Soluto y Solvente con Densidad)
Calcular la molalidad de 5.00 g de Urea (CH4N2O) disueltos en
50.0 mL de Agua.
Datos: Masa Molar Urea = 60.1 g/mol; Densidad del agua = 1.00 g/mL.
Procedimiento:
Opción Fórmula: m = n / kg
Opción Recomendada: Línea de
Razonamiento (uso seguro de densidad).
Razonamiento: Similar al Ejemplo 1, usamos la densidad para transformar el volumen de agua a masa.
| 5.00 g Urea | x | 1 mol Urea | x | 1 mL Agua | x | 1000 g Agua | = 1.66 m |
| 50.0 mL Agua | 60.1 g Urea | 1.00 g Agua | 1 kg Agua |
Calculando Masa de Soluto (Despejes)
En estos casos, conocemos la concentración (m) y la cantidad de solvente, y buscamos cuántos gramos de soluto se necesitan.
Ejemplo N° 4 (Soluto Sólido, Solvente en Kg)
¿Cuántos gramos de KCl (Cloruro de Potasio) se necesitan para preparar una solución
0.500 m usando 2.00 kg de Agua?
Datos: Masa Molar KCl = 74.6 g/mol.
Procedimiento:
Opción Fórmula: Despejar de m = n /
kg (requiere álgebra).
Opción Recomendada: Línea de
Razonamiento (factor unitario).
Razonamiento: Partimos del solvente disponible y usamos la molalidad como factor de conversión (0.500 mol KCl / 1 kg Agua) para llegar a moles, y finalmente a gramos.
| 2.00 kg Agua | x | 0.500 mol KCl | x | 74.6 g KCl | = 74.6 g KCl |
| 1 kg Agua | 1 mol KCl |
Ejemplo N° 5 (Soluto Sólido, Solvente en Gramos)
Calcular la masa de Sacarosa (C12H22O11) necesaria
para preparar una solución 0.250 m con 500. g de Agua.
Datos: Masa Molar Sacarosa = 342. g/mol.
Procedimiento:
Opción Fórmula: Despejar n (y luego g) de m
= n / kg
Opción Recomendada: Línea de
Razonamiento (conversión directa).
Razonamiento: Primero convertimos el agua a kg, luego usamos la molalidad para hallar moles, y finalmente a gramos con la masa molar.
| 500. g Agua | x | 1 kg Agua | x | 0.250 mol Sac | x | 342. g Sac | = 42.8 g Sacarosa |
| 1000 g Agua | 1 kg Agua | 1 mol Sac |
Ejemplo N° 6 (Soluto Sólido, Solvente en Volumen)
Se requiere preparar una solución de Ácido Ascórbico (Vit C,
C6H8O6) al 1.20 m usando 250. mL de Agua.
¿Cuántos gramos de vitamina C necesitamos?
Datos: Masa Molar Vit C = 176. g/mol; Densidad Agua = 1.00 g/mL.
Procedimiento:
Opción Fórmula: Despejar de m = n /
kg
Opción Recomendada: Línea de
Razonamiento (incluyendo densidad).
Razonamiento: Iniciamos con el volumen, pasamos a masa (densidad), luego a kg, de ahí a moles (usando m) y finalmente a gramos.
| 250. mL Agua | x | 1.00 g Agua | x | 1 kg Agua | x | 1.20 mol VitC | x | 176. g VitC | = 52.8 g Vit C |
| 1 mL Agua | 1000 g Agua | 1 kg Agua | 1 mol VitC |
Calculando Masa de Solvente (Despejes para Agua)
En ocasiones la pregunta es inversa: ¿Cuánta agua necesito para disolver cierta cantidad de soluto y lograr una concentración específica?
Ejemplo N° 7 (Datos en Moles, Solvente en kg)
¿Qué masa de agua (en kg) se necesita para disolver 0.750 moles de NaCl y obtener una solución 0.250 m?
Procedimiento:
Razonamiento: Usamos la molalidad como factor de conversión, pero invertido (1 kg / 0.250 mol), para cancelar los moles y obtener kg.
| 0.750 mol NaCl | x | 1 kg Agua | = 3.00 kg Agua |
| 0.250 mol NaCl |
Ejemplo N° 8 (Datos en Gramos, Solvente en Gramos)
Se desean preparar una solución 0.800 m de Sulfato Cúprico (CuSO4).
Si se usan 25.0 g de soluto, ¿cuántos gramos de agua se requieren?
Datos: Masa Molar CuSO4 = 159.6 g/mol.
Procedimiento:
Razonamiento: Realizamos todo en una sola línea. Convertimos los gramos de soluto a moles y simultáneamente usamos la molalidad para encontrar la masa de solvente.
| 25.0 g CuSO4 | x | 1 mol CuSO4 | x | 1 kg Agua | x | 1000 g Agua | = 196 g Agua |
| 159.6 g CuSO4 | 0.800 mol | 1 kg Agua |
Ejemplo N° 9 (Contexto Real - Anticongelante)
Para evitar que un motor se congele, se prepara una solución de Etilenglicol
(C2H6O2) al 1.50 m. Si se agregan 200. g
(el punto decimal indica 3 cifras
significativas) de Etilenglicol, ¿cuántos gramos de agua deben usarse?
Datos: Masa Molar Etilenglicol = 62.1 g/mol.
Procedimiento:
Razonamiento: Convertimos de gramos de soluto a moles y luego a kilogramos de solvente en un solo paso continuo.
| 200. g Etilenglicol | x | 1 mol EG | x | 1 kg Agua | x | 1000 g Agua | = 2150 g Agua |
| 62.1 g EG | 1.50 mol | 1 kg Agua |
I. Calculando Molalidad (m)
1. Etanol en Agua
Se disuelven 25.0 g de Etanol (C2H5OH, MM=46.07 g/mol) en 200. g de agua. Calcule la molalidad.
Línea de Razonamiento:
Configuramos la relación inicial (masa soluto / masa solvente) y aplicamos factores de conversión para transformar ambas unidades simultáneamente a moles y kg respectivamente.
| 25.0 g Etanol | x | 1 mol Etanol | x | 1000 g Agua | = 2.71 m |
| 200. g Agua | 46.07 g Etanol | 1 kg Agua |
2. Cloruro de Potasio
Si disolvemos 15.0 g de KCl (MM=74.55 g/mol) en 0.500 kg de agua, ¿cuál es la concentración molal?
Línea de Razonamiento:
El solvente ya está en kg, así que solo aplicamos un factor de conversión para cambiar los gramos de soluto a moles.
| 15.0 g KCl | x | 1 mol KCl | = 0.402 m |
| 0.500 kg Agua | 74.55 g KCl |
3. Urea (con volumen)
Se disuelven 5.00 g de Urea (CH4N2O, MM=60.06 g/mol) en 75.0 mL de agua (d=1.00 g/mL). Calcule la molalidad.
Línea de Razonamiento:
Debemos transformar:
1. Gramos de Urea → Moles.
2. Mililitros de Agua → Gramos → Kilogramos.
| 5.0 g Urea | x | 1 mol Urea | x | 1 mL Agua | x | 1000 g Agua | = 1.11 m |
| 75.0 mL Agua | 60.06 g Urea | 1.00 g Agua | 1 kg Agua |
II. Calculando Masa de Soluto (g)
4. Hidróxido de Sodio
¿Cuántos gramos de NaOH (MM=40.0 g/mol) se necesitan para preparar una solución 0.500 m usando 2.0 kg de agua?
Línea de Razonamiento:
Partimos de la masa de solvente (kg) y usamos la molalidad como factor de conversión (mol soluto / kg solvente) para obtener moles, y finalmente gramos.
| 2.0 kg Agua | x | 0.500 mol NaOH | x | 40.0 g NaOH | = 40.0 g NaOH |
| 1 kg Agua | 1 mol NaOH |
5. Metanol
Se requiere una solución 1.20 m de Metanol (CH3OH, MM=32.04 g/mol) utilizando 500. g de agua. ¿Masa de soluto?
Línea de Razonamiento:
El agua está en gramos, así que primero la convertimos a kg, luego usamos la molalidad para obtener moles, y finalmente la masa molar para obtener gramos.
| 500 g Agua | x | 1 kg Agua | x | 1.20 mol Met | x | 32.04 g Met | = 19.2 g Metanol |
| 1000 g Agua | 1 kg Agua | 1 mol Met |
6. Sacarosa
Prepare una solución 0.10 m de Sacarosa (C12H22O11, MM=342.3 g/mol) en 100. g de agua. ¿Cuántos gramos pesará?
Línea de Razonamiento:
Mismo proceso: convertir agua a kg → usar molalidad → convertir a gramos.
| 100 g Agua | x | 1 kg Agua | x | 0.10 mol Sac | x | 342.3 g Sac | = 3.42 g Sacarosa |
| 1000 g Agua | 1 kg Agua | 1 mol Sac |
III. Calculando Masa de Solvente (kg)
7. Salmuera (NaCl)
Tienes 5.0 moles de NaCl y deseas preparar una solución 2.0 m. ¿Cuántos kg de agua necesitas?
Línea de Razonamiento:
Usamos la molalidad como factor de conversión invertido (kg solvente / mol soluto) para cancelar los moles y obtener la masa del solvente.
| 5.0 mol NaCl | x | 1 kg Agua | = 2.5 kg Agua |
| 2.0 mol NaCl |
8. Glucosa
¿Cuántos kg de agua se necesitan para disolver 90.0 g de Glucosa (C6H12O6, MM=180 g/mol) y obtener una solución 0.500 m?
Línea de Razonamiento:
Convertimos gramos de soluto a moles, y luego usamos la molalidad invertida para hallar los kilogramos de agua necesarios.
| 90.0 g Glu | x | 1 mol Glu | x | 1 kg Agua | = 1.00 kg Agua |
| 180 g Glu | 0.500 mol Glu |
9. Hidróxido de Potasio (KOH)
Deseas una solución diluida de 0.0100 m de KOH usando 0.561 g de soluto (MM=56.1 g/mol). ¿Cuántos kg de agua agregas?
Línea de Razonamiento:
Similar al anterior: g KOH → mol KOH → kg Agua (usando 0.0100 m invertido).
| 0.561 g KOH | x | 1 mol KOH | x | 1 kg Agua | = 1.00 kg Agua |
| 56.1 g KOH | 0.0100 mol KOH |